- 진피 줄기세포, 출생 직후 유전자발현 급변해 모낭생성능력 소실
- 핵심원인은 ‘Twist2 전사인자’...후생유전적 염색질 재구조화 유발
- Twist2 전사인자 조절하면 성인기에도 모낭 생성 가능성 있어
사진 표
|

|
|
|
[사진 왼쪽부터] 피부과 권오상, 조성진 교수 |
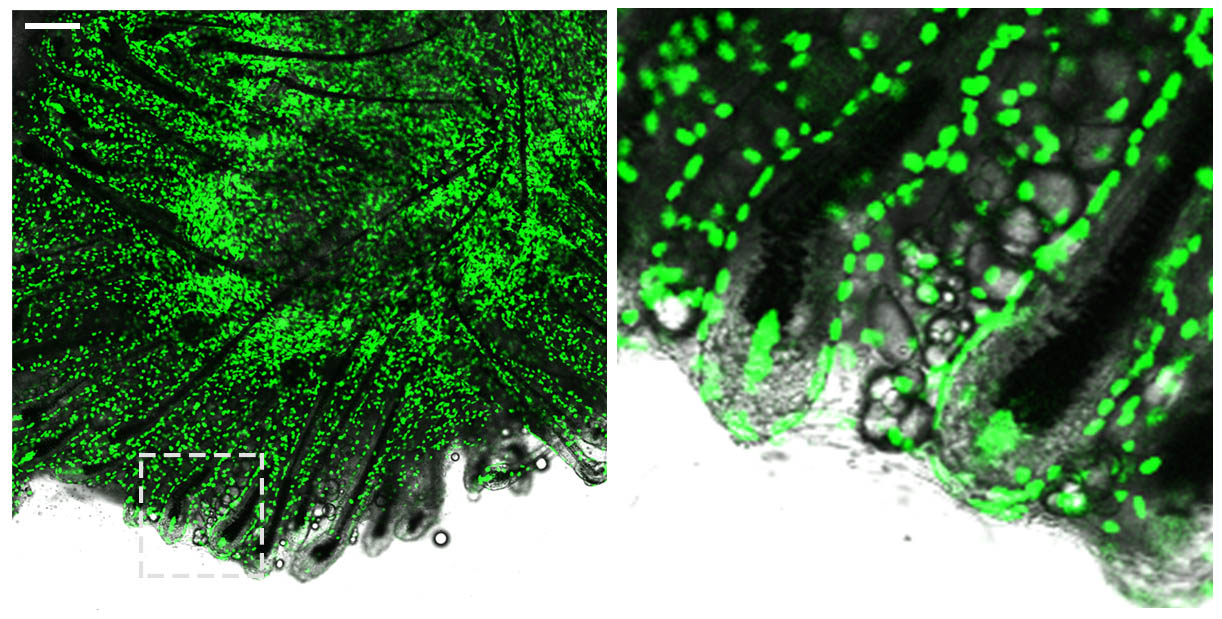
[자료1] 재생된 모낭 확대 사진. 모낭은 성체줄기세포인
상부진피 섬유아세포(녹색 영역)로부터 만들어지고 있었다. |
태아 때만 갖고 있는 모낭 재생능력을 성인의 피부에서도 회복할 수 있는 가능성이 제시됐다. 국내 연구진이 모낭 재생능력의 소실 과정과 핵심인자를 최초로 규명해냈다.
서울대병원 피부과 권오상·조성진 교수 연구팀(김진용 박사, 박민지 박사과정)은 태아기 모낭 생성을 담당하는 성체 줄기세포인 ‘상부진피 섬유아세포’를 대상으로 출생 직후 모낭 재생능력이 사라지는 기전에 대해 연구한 결과를 7일 밝혔다.
모낭은 태아기 3~7개월에 완성된 후 더 이상 생성되지 않는다. 모낭 생성을 담당하는 진피 줄기세포가 출생 후 기존의 모낭 재생능력을 잃어버리기 때문이다. 그러므로 사는 동안 모낭에 손상을 입으면 그 개수가 줄어 영구적인 탈모로 이어지게 된다.
연구팀은 출생 후 진피 줄기세포에서 모낭 재생능력이 사라지는 기전을 확인하고 원인을 찾기 위해 쥐의 진피 줄기세포인 ‘상부진피 섬유아세포(이하 섬유아세포)’를 분석했다.
그러자 섬유아세포의 모낭 재생능력은 출생 직후 급격히 감소하여 생후 4일째 완전히 없어지는 것으로 나타났다.
이처럼 급격한 변화의 원인을 찾기 위해 섬유아세포의 유전자 발현 양상을 날짜별로 확인한 결과, 세포를 성숙시키는 유전자 발현은 급증한 반면 재생능력과 관련된 것은 급감하는 모습이 관찰됐다.
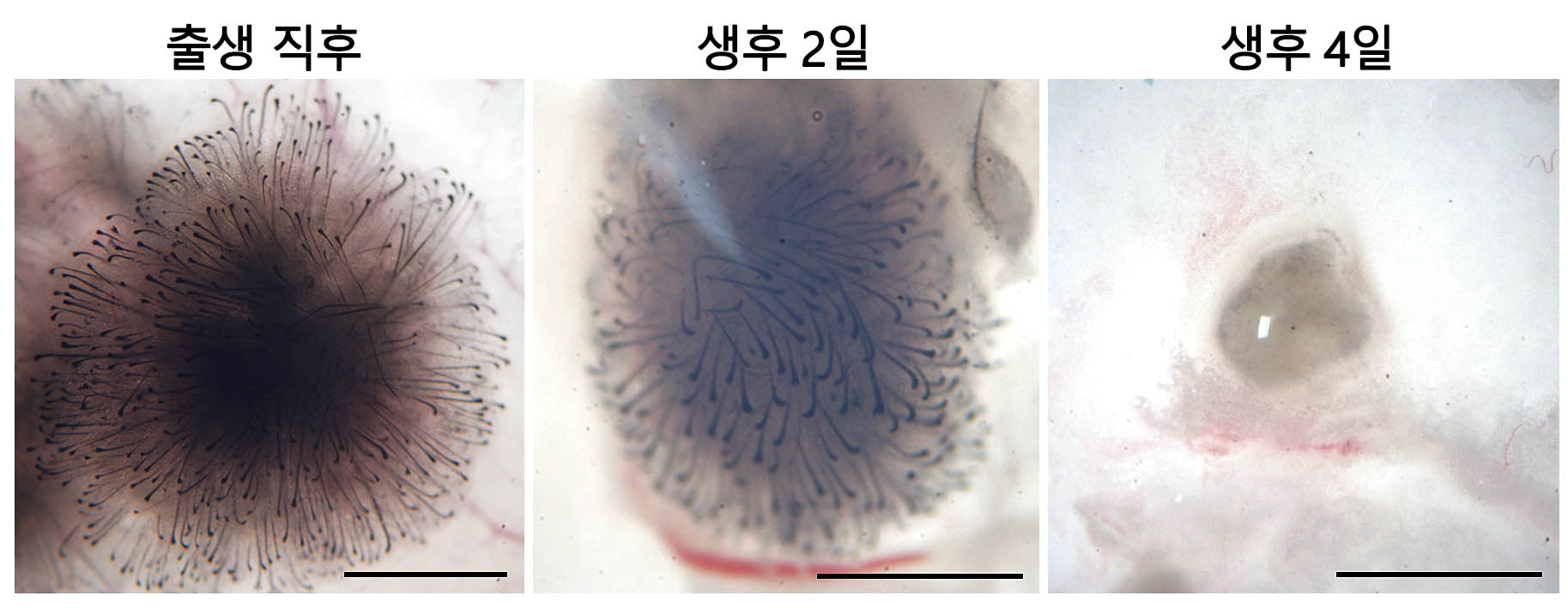
[자료2] 생후 0~4일째 섬유아세포 모습 비교. 섬유아세포는 생후 4일 만에
모낭 재생능력을 완전히 잃고 세포덩어리 형태로 변했다.
연구팀은 불과 4일 만에 유전자 발현 양상이 급변한 원인을 후생유전적 조절 기전의 일종인 ‘히스톤 단백질 탈아세틸화’에서 찾았다.
후생유전적 조절 기전은 DNA 염기서열의 변형 없이, 스위치처럼 유전자 발현을 열고 닫는 조절을 통해 유전자 발현 패턴이 변하는 것을 말한다.
출생 직후 발생한 히스톤 단백질 탈아세틸화 현상은 섬유아세포 내 염색질 재구조화를 일으켰고, 이로 인해 재생능력 관련 유전자 발현이 감소하는 방향으로 전반적인 발현 패턴이 변화했다.
반면 의도적으로 탈아세틸화를 억제한 경우 염색질 재구조화가 발생하지 않아서 유전자 발현 패턴에 변화가 없었다. 그에 따라 섬유아세포의 모낭 재생능력도 유지되는 것으로 나타났다.
나아가 연구팀은 이 기전의 핵심 조절인자를 확인하기 위해 추가 실험을 진행했으며, ‘Twist2 전사인자’가 탈아세틸화를 유발하는 효소와 결합해 염색질 재구조화를 조절한다는 사실을 확인했다.
이를 바탕으로 Twist2 전사인자가 섬유아세포의 모낭 재생능력이 소실되는 기전에 있어서 결정적으로 관여하는 ‘마스터 조절자’라고 연구팀은 결론지었다.
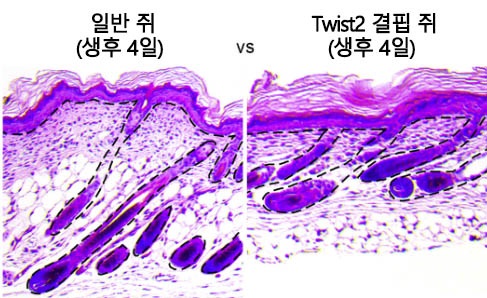
[자료3] Twist2 전사인자가 결핍된 쥐와 일반 쥐의 피부 비교.
Twist2 전사인자가 결핍된 쥐는 일반 쥐보다 다수의 진피 줄기세포가 빽빽하게 밀집되고
지방층을 포함한 피부 두께는 얇았으나, 표피와 모낭 조직은 계속 자라나고 있었다.
이번 연구는 그동안 정확히 알려진 바 없었던 진피 줄기세포의 모낭 재생능력 소실 기전을 최초로 규명했다는 점에서 중요한 성과다.
특히 마스터 조절자인 Twist2 전사인자를 조절해 성인기에도 모낭 재생능력을 활성화시킬 수 있다는 가능성을 제시하여 의미가 크다고 연구팀은 강조했다.
피부과 권오상 교수는 “연구로 밝혀진 기전을 활용한다면 성인기에도 모낭을 갖춘 온전한 피부를 재생할 수 있을 것으로 기대된다”며, “이 결과는 영구 탈모를 겪고 있거나 피부 조직이 심하게 손상된 환자들에게 재생의학 관점에서 새로운 치료의 길을 열어줄 것”이라고 말했다.
이번 연구는 과학기술정보통신부 한국연구재단 중견연구과제의 지원으로 이뤄졌으며, 셀 학술지의 오픈 액세스 저널인 ‘셀 리포트(Cell Reports)’에 온라인 게재됐다.



